创新生物药的获批数量反超美国
FDA批准的创新生物药定义为以351途径首次获批的BLA申请;NMPA的定义为通用名首次获批的进口原研,以及审评时以治疗用或预防用生物制品1类申报的商品。数据显示,2016年到2018年中国创新生物药的获批数量增长明显,在2018年开始接近美国,从2019年起获批数量反超美国,19年和20年的获批数量都比美国的多4-5个。
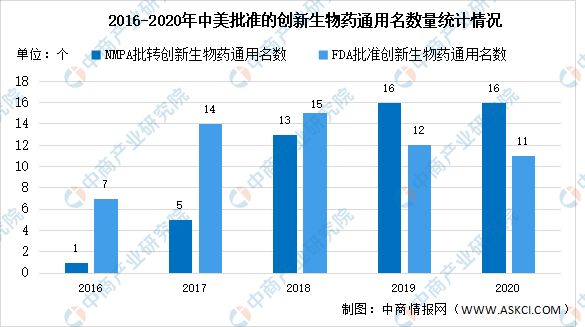
数据来源:医药地理、中商产业研究院整理
与申报类似,获批占比最大的仍然是抗肿瘤药,达到30%。占比前5的其他治疗类别分别是骨骼肌肉用药、消化系统用药、内分泌及代谢调节用药、以及皮肤科用药。
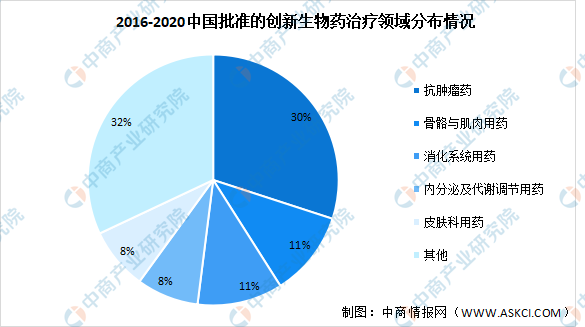
数据来源:医药地理、中商产业研究院整理
抗体类药物是获批的主流技术类别,占比达到了获批通用名的61%。靶向药占到了所有通用名的82%,这些靶向药所针对的靶点中,靶向PD1和PDL1的通用名是最多的,另外还有一些TNF-α、HER2等“网红靶点”。
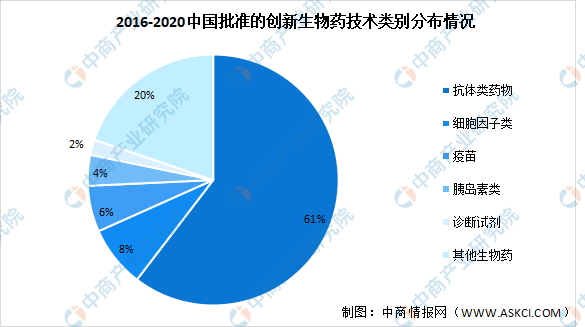
数据来源:医药地理、中商产业研究院整理
 如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。
如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。

